(腎細胞癌に対する承認内容)
バベンチオ®効能又は効果:根治切除不能又は転移性の腎細胞癌
安全性・適正使用情報
副作用
臨床試験における副作用情報
JAVELIN Renal 101試験:国際共同第Ⅲ相試験(B9991003試験)1)
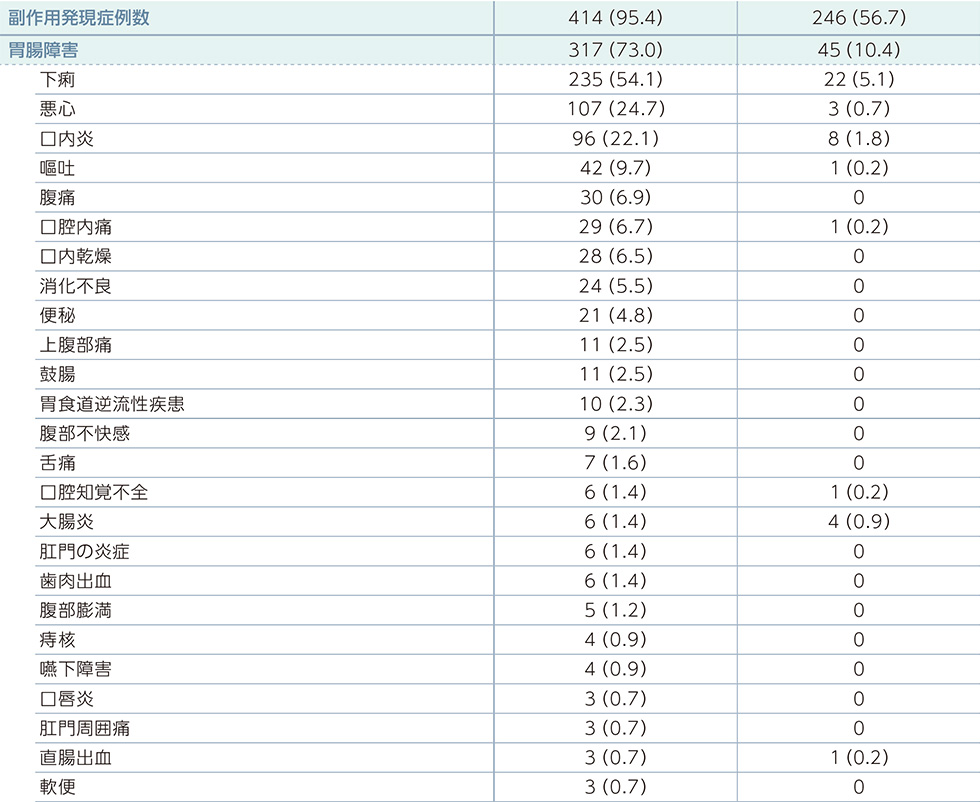
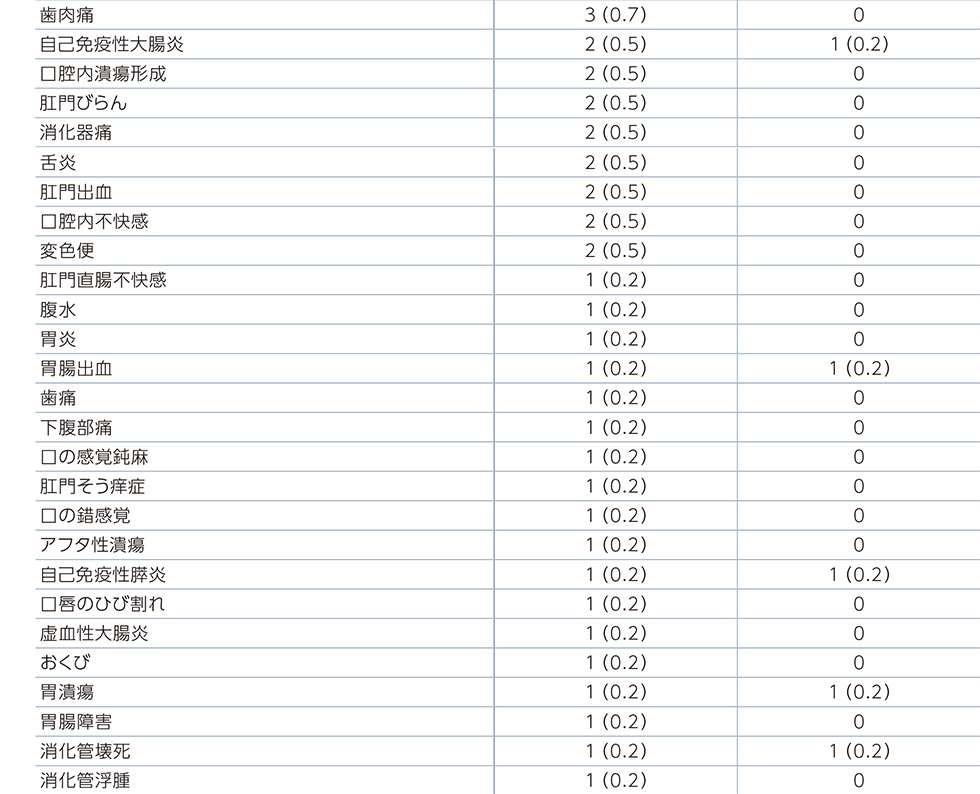
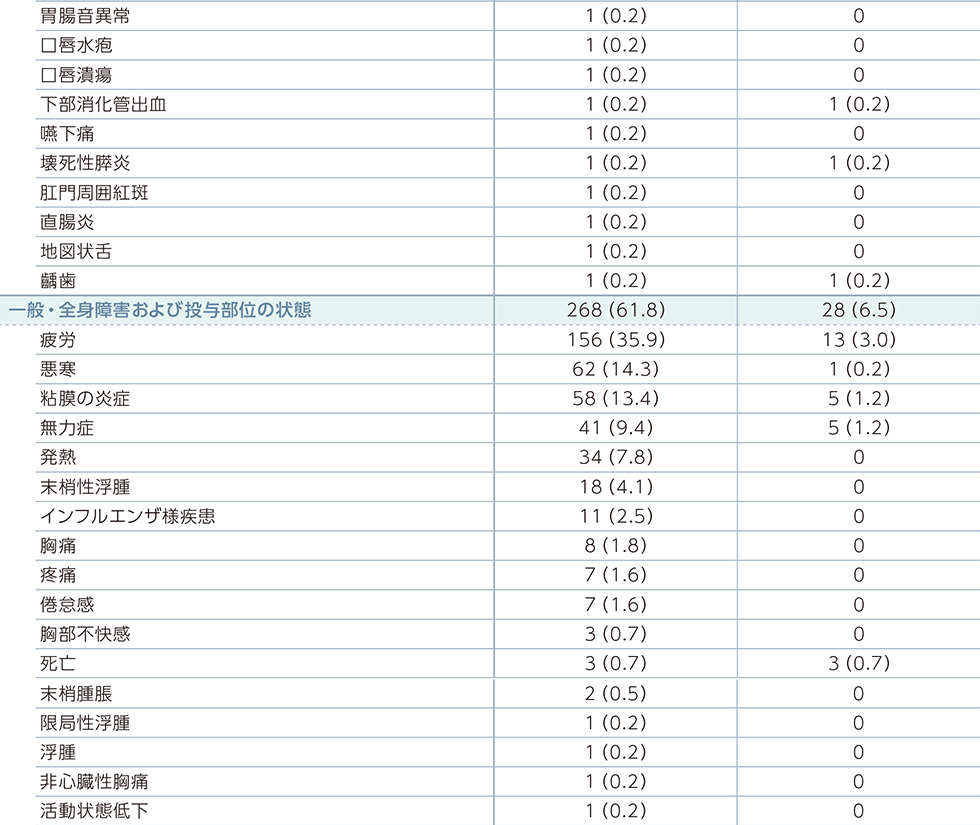
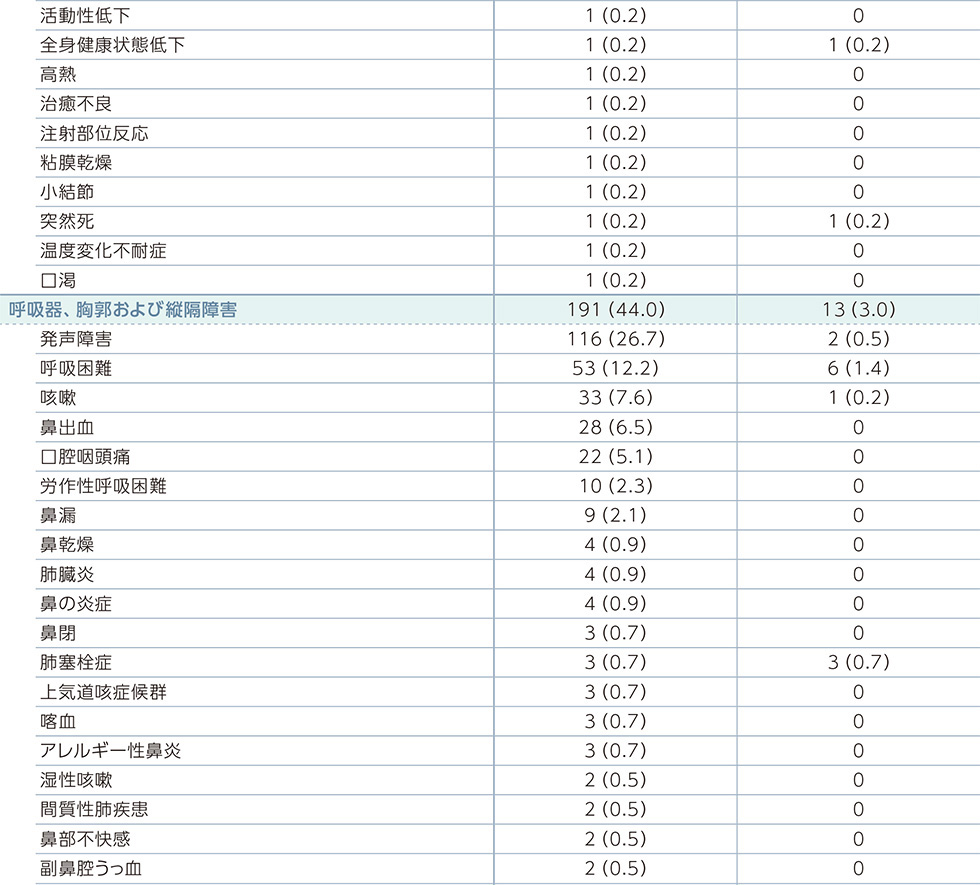
JAVELIN Renal 101試験:国際共同第Ⅲ相試験(B9991003試験)において、バベンチオ®+アキシチニブ併用投与を受けた434例(日本人*1 33例を含む)中414例(95.4%)に副作用が認められました。(効能又は効果追加承認時)(PFS最終解析時点)
*1:日本の治験実施施設で治験に参加した患者(全患者集団に中国人1例、その他のアジア人1例を含む)
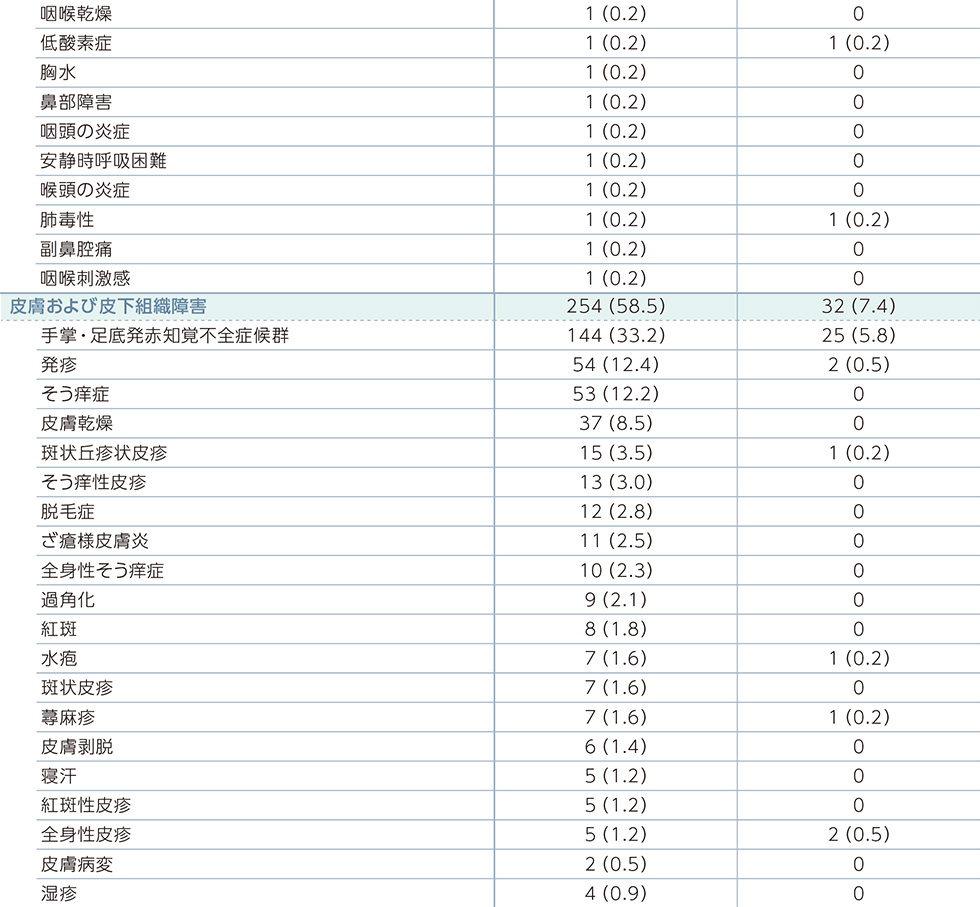
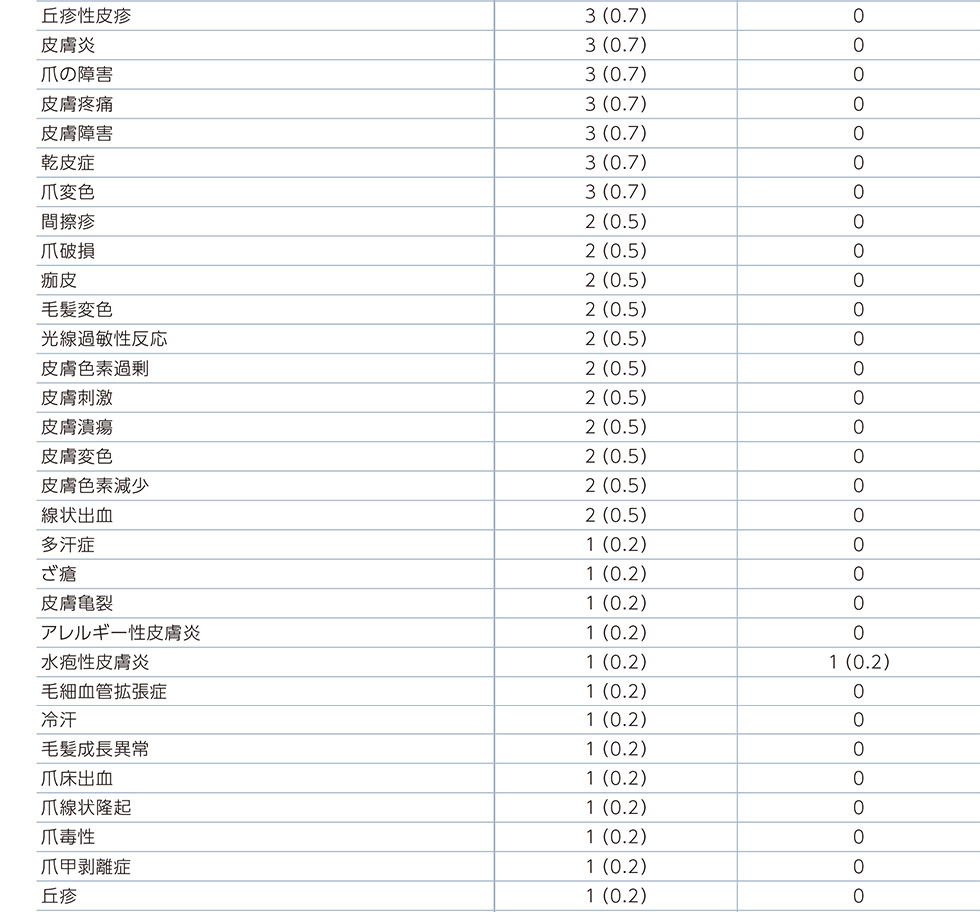
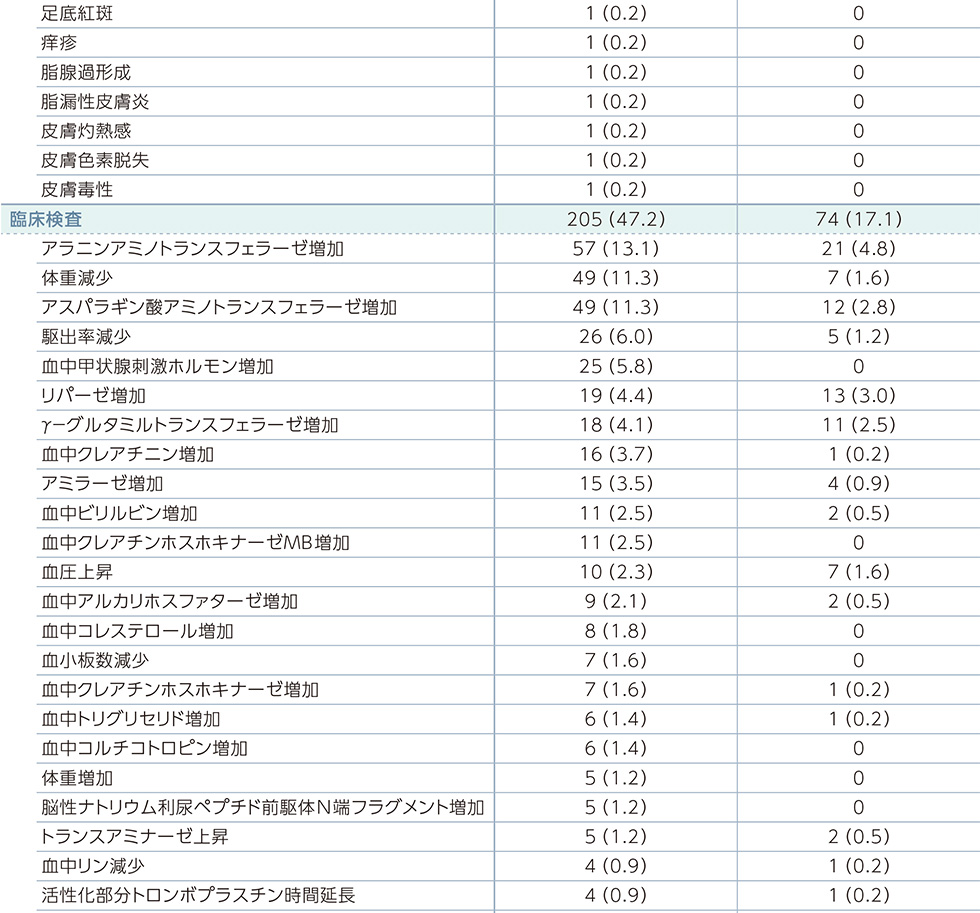
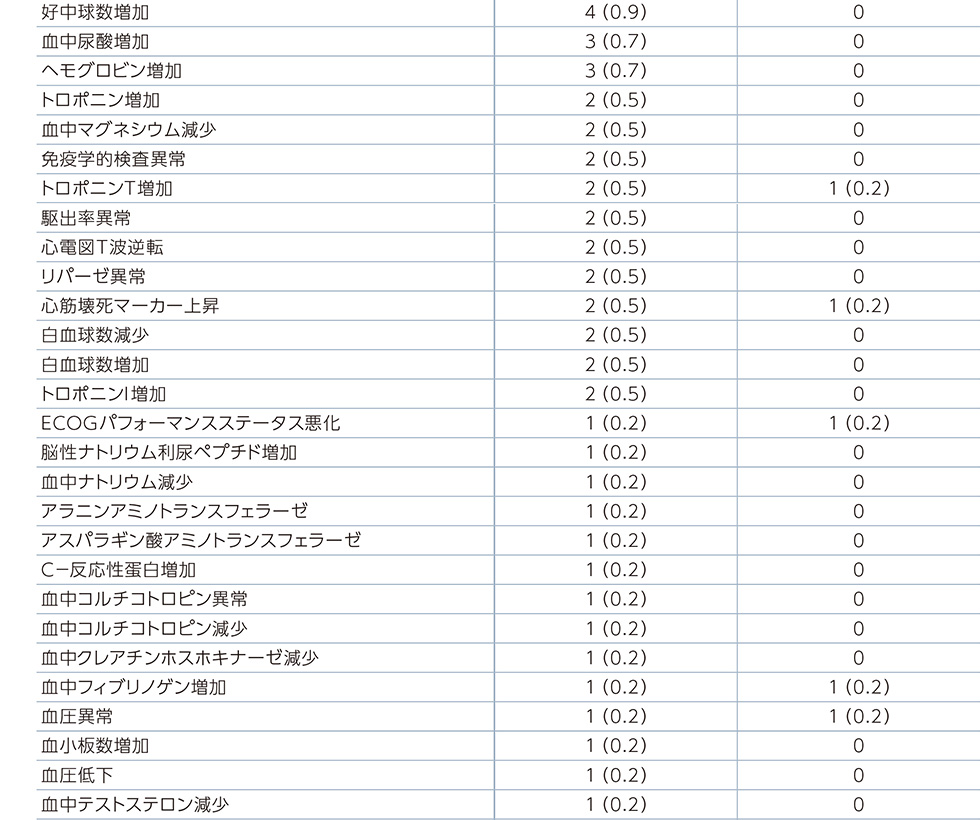
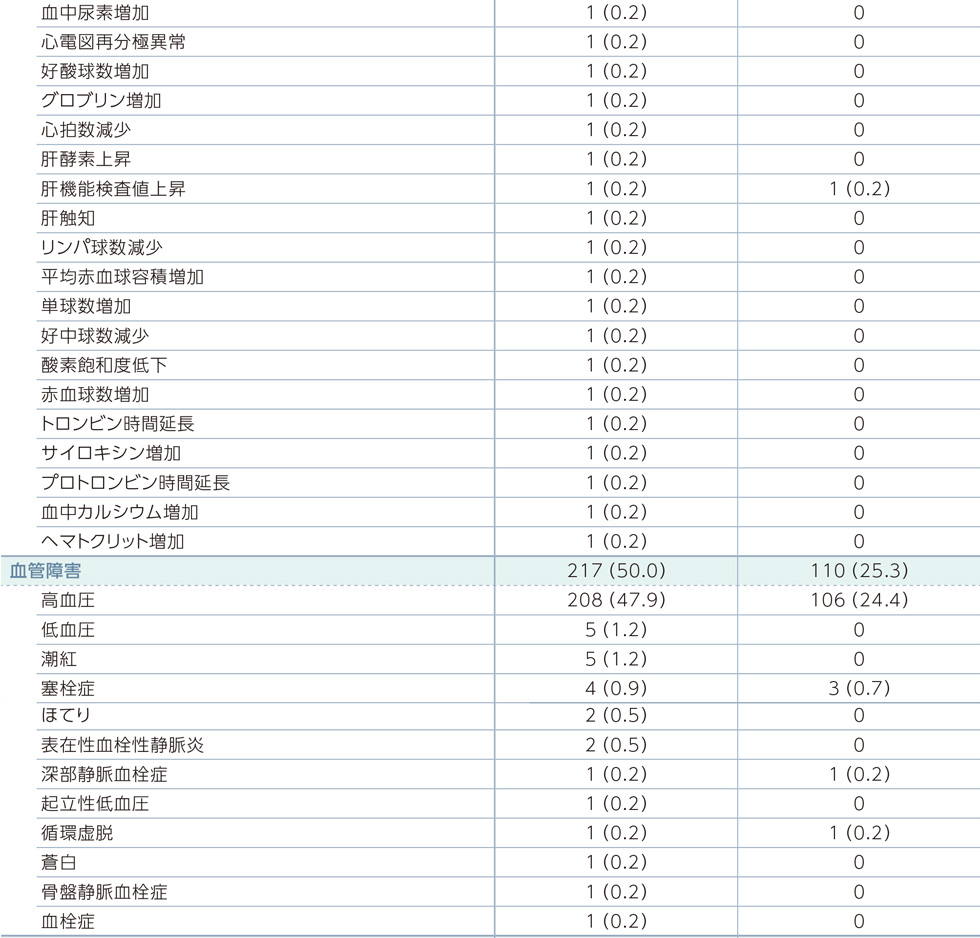
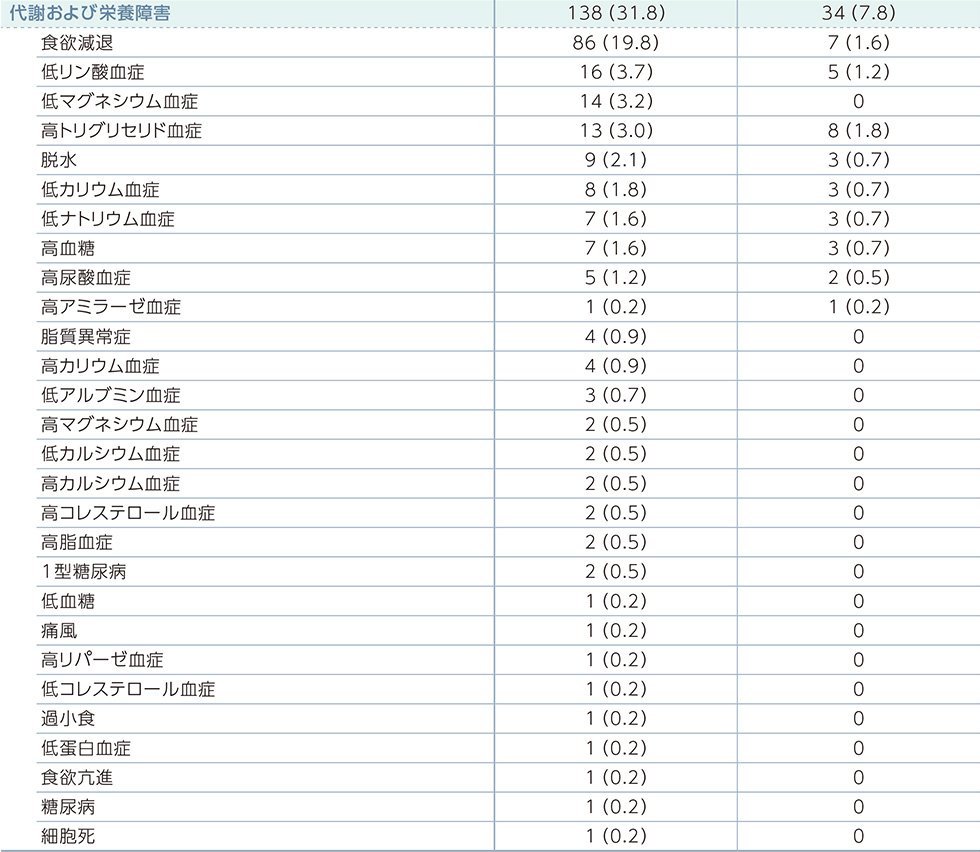
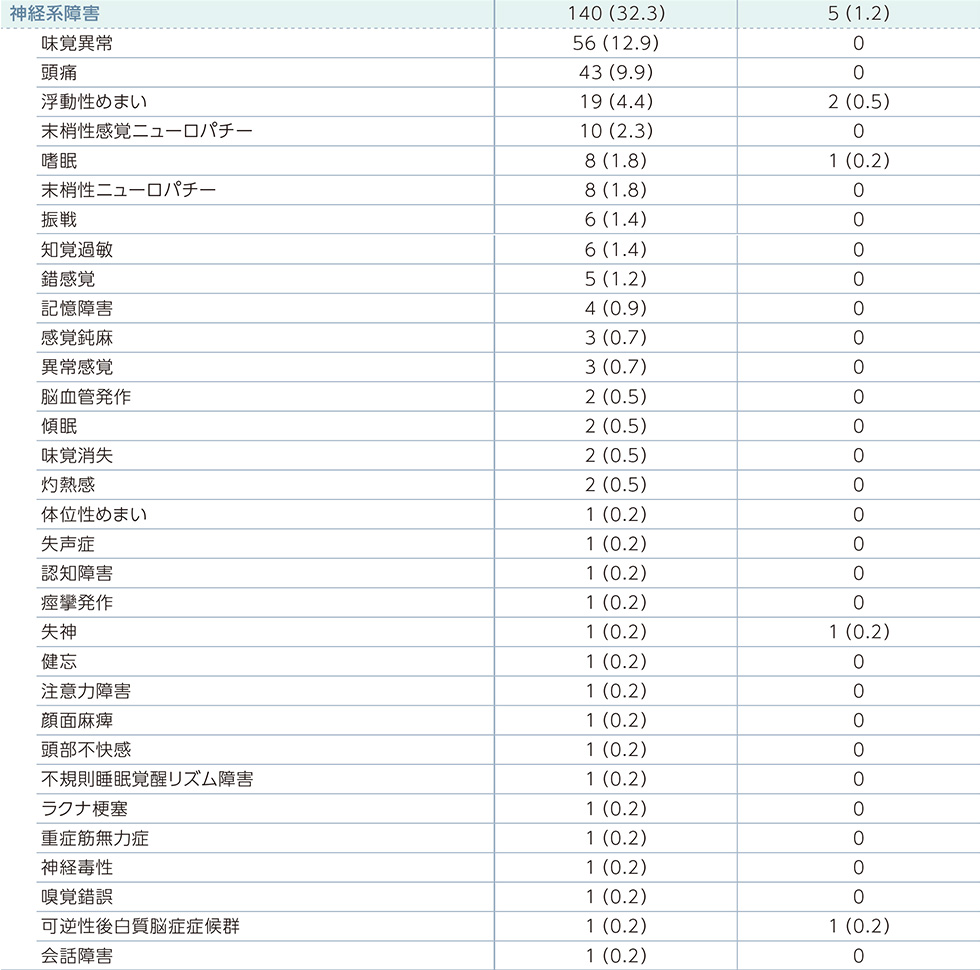
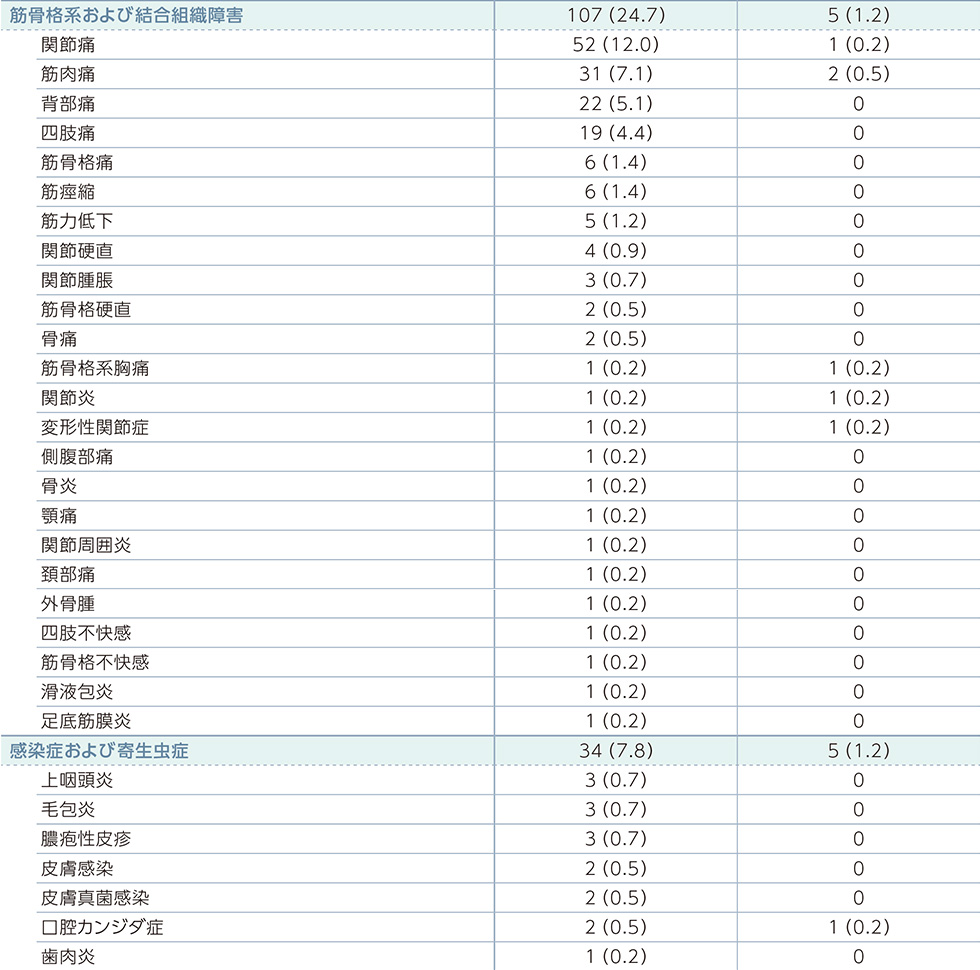
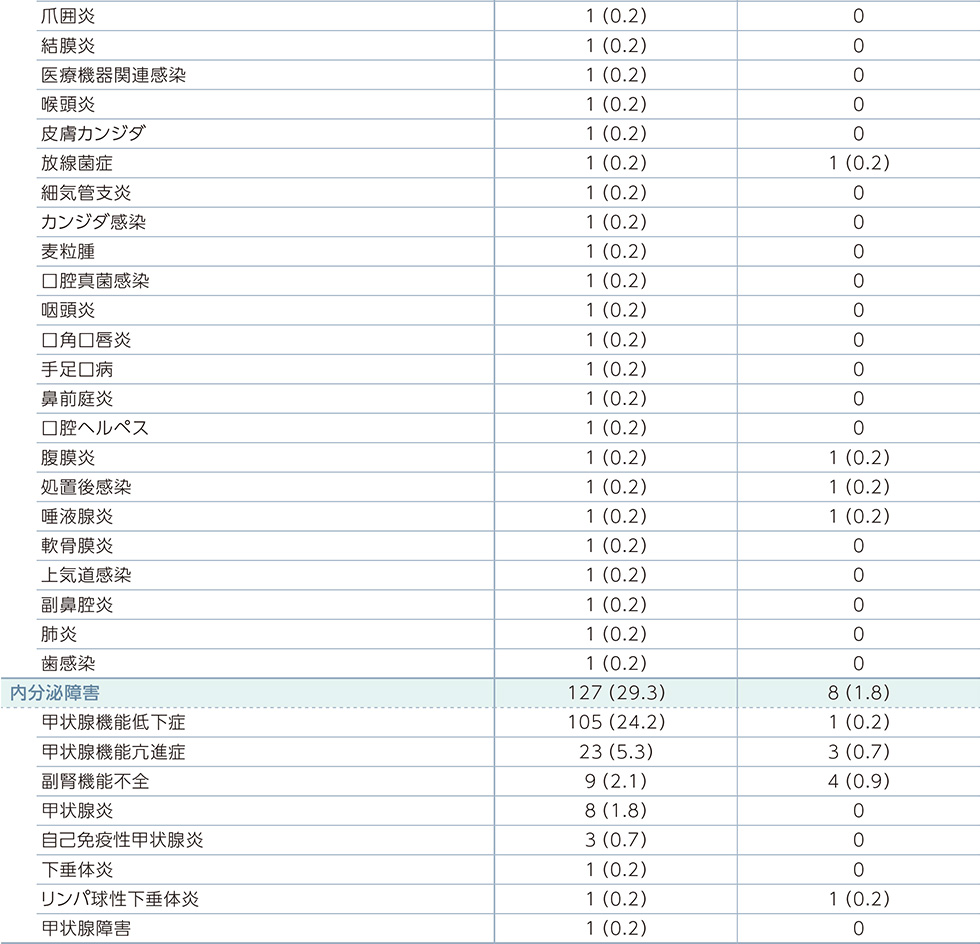
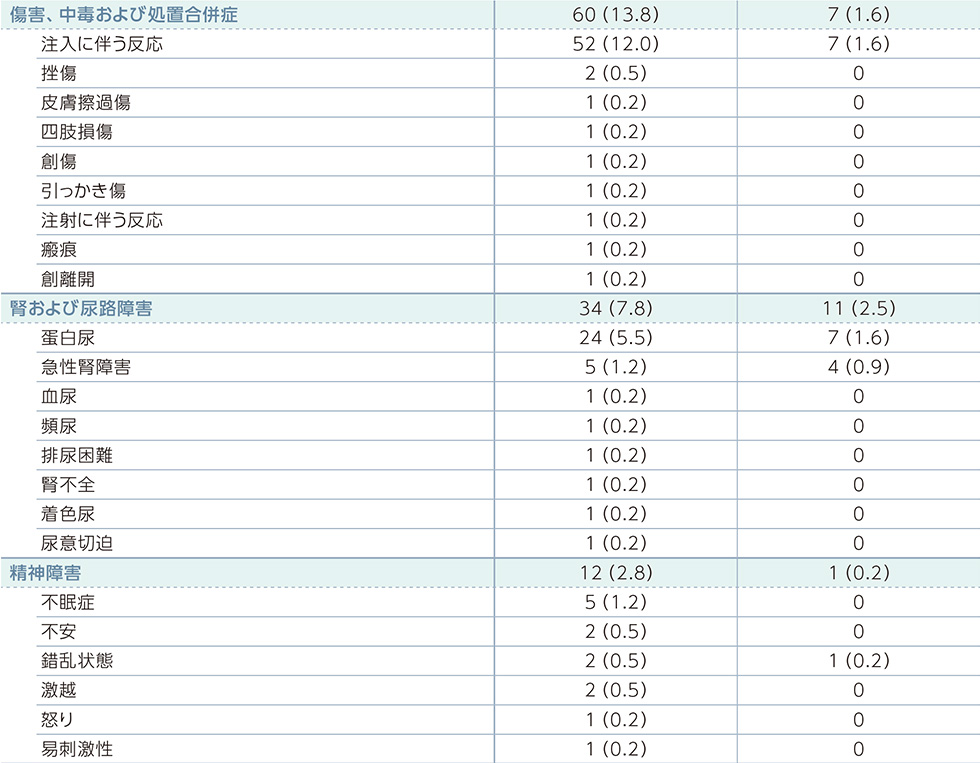
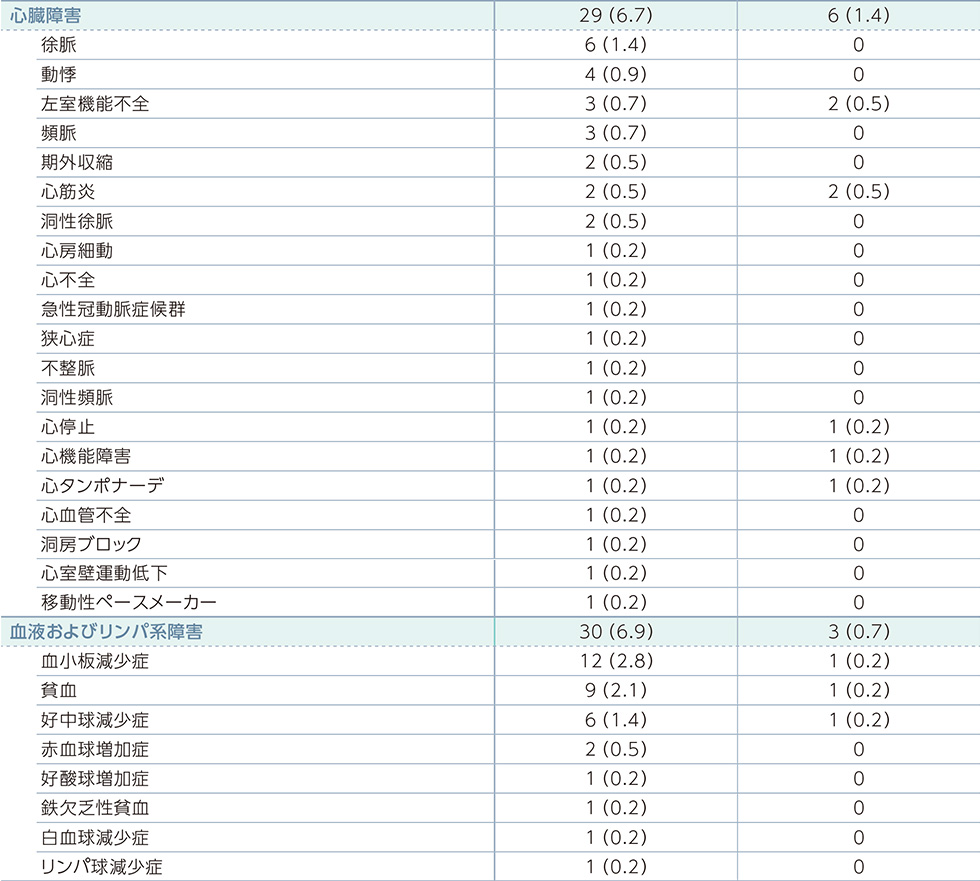
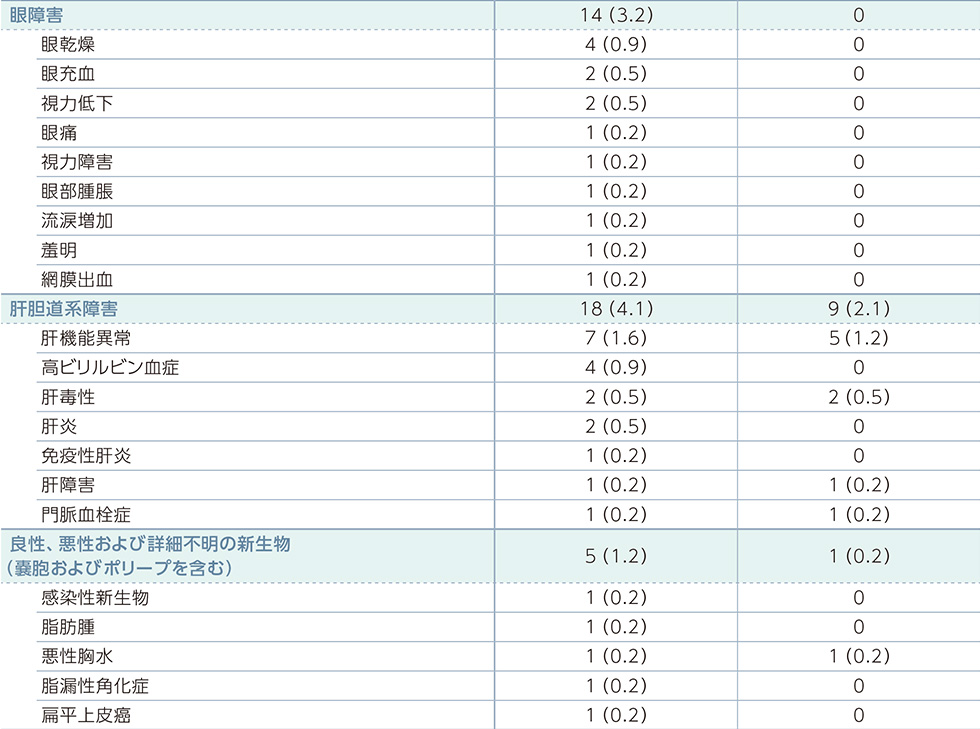
副作用一覧(PFS最終解析時点)
| 安全性評価対象例数 | 434例 |
|---|---|
| 副作用発現例数(発現率) | 414例(95.4%) |
MedDRA器官別大分類及び基本語別副作用発現状況*2
MedDRA Version 21.0 器官別大分類及び基本語別の治験薬との因果関係が否定できない有害事象、GradeはNCI-CTCAE v4.03に準じる。
*2:効能又は効果追加承認申請時評価資料に基づき集計した。
1)社内資料:国際共同第Ⅲ相試験(B9991003試験)(2019年12月承認、CTD 2.7.6.1)承認時評価資料
市販後の副作用情報
本剤承認日以降に当社で入手した市販後症例*の情報に基づき、まとめられた市販後安全性情報の一覧表になります。当該安全性情報は月次で更新しております。
*自発報告、文献報告、使用成績調査等からの情報は含まれますが、製造販売後臨床試験からの情報は含めていません。
なお、記載されている情報は、速報性を重視するために調査の完了・未完了にかかわらず掲載をしておりますので、今後入手する情報などで内容・評価が変更されることがあります。
2023年11月 JP-AVE-00931